En esta ocasión hablaremos del petróleo.
Se sabe que el petróleo es un compuesto de hidrocarburos, es inflamable, más ligero que el agua de color negro o verde obscuro.
A ciencia cierta no se sabe cual es su origen pero se cree que es una materia orgánica de restos de animales o algas
Para encontrar petróleo es necesario un estudio geológico se obtiene penetrando pozos de 30 a 50 cm de diámetro y de 100 a 700 metros de profundidad.
Química Industrial
martes, 29 de enero de 2013
sábado, 3 de noviembre de 2012
Actividad experimental: Determinación del pH
UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO
COLEGIO DE CIENCIA Y HUMANIDADES PLANTEL VALLEJO
ACTIVIDAD EXPERIMENTAL
Objetivo:Comprobar y conocer el pH de los materiales a explorar.
Introducción: El pH (potencial de hidrógeno) es una medida de acidez o alcalinidad de una disolución. El pH indica la concentración de iones hidronio [H3O+] presentes en determinadas sustancias.
Escala de pH
Los ácidos y las bases tienen una característica que permite medirlos: es la concentración de los iones de hidrógeno (H+). Los ácidos fuertes tienen altas concentraciones de iones de hidrógeno y los ácidos débiles tienen concentraciones bajas. El pH, entonces, es un valor numérico que expresa la concentración de iones de hidrógeno.
Hay centenares de ácidos. Ácidos fuertes, como el ácido sulfúrico, que puede disolver los clavos de acero, y ácidos débiles, como el ácido bórico, que es bastante seguro de utilizar como lavado de ojos. Hay también muchas soluciones alcalinas, llamadas "bases", que pueden ser soluciones alcalinas suaves, como la Leche de Magnesia, que calman los trastornos del estómago, y las soluciones alcalinas fuertes, como la soda cáustica o hidróxido de sodio, que puede disolver el cabello humano.
Los valores numéricos verdaderos para estas concentraciones de iones de hidrógeno marcan fracciones muy pequeñas, por ejemplo 1/10.000.000 (proporción de uno en diez millones). Debido a que números como este son incómodos para trabajar, se ideó o estableció una escala única. Los valores leídos en esta escala se llaman las medidas del "pH".
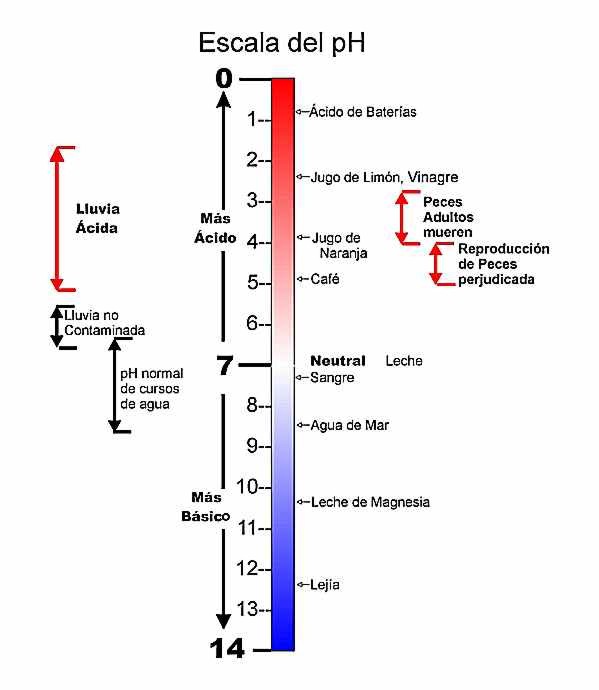 |
• La escala pH está dividida en 14 unidades, del 0 (la acidez máxima) a 14 ( nivel básico máximo). El número 7 representa el nivel medio de la escala, y corresponde al punto neutro. Los valores menores que 7 indican que la muestra es ácida. Los valores mayores que 7 indican que la muestra es básica.
• La escala pH tiene una secuencia logarítmica, lo que significa que la diferencia entre una unidad de pH y la siguiente corresponde a un cambio de potencia 10. En otras palabras, una muestra con un valor pH de 5 es diez veces más ácida que una muestra de pH 6. Asimismo, una muestra de pH 4 es cien veces más ácida que la de pH 6.
Materiales:
- 10 sustancias de uso común
- Tubos de ensalle y base
- Laminas pH
- Agua destilada
Procedimiento: En cada tubo de ensalle se vierte la sustancia y se le agrega agua destilada. Debe hacerse una mezcla homogénea, si es necesario se tiene que agitar hasta conseguir la mezcla.
Una vez finalizada esta etapa, procedemos a tomar una de las laminillas pH, vertir en el tubo en que se encuentra la sustancia, esperar el resultado.
La laminilla marcara una serie de colores y con ellos sabremos cual es el pH de cada sustancia.
Evidencia Fotográfica:
Análisis de Resultados:
Sustancias a las cuales calculamos su pH:
- Perfume ------- 5
- Alcohol----------6
- Vinagre----------2
- Aceite------------6
- Suavitel---------10
- Shampoo-------6
- Crema Corporal 6
- Enjuague Capilar 5
- Agua-------------7
- Jabón de Manos 6
- Yogurt bebible 4
Conclusión: Debemos saber el pH de las cosas básicas de nuestro uso cotidiano para tener o estar equilibrados.
Velocidad de Reacción
VELOCIDAD DE REACCIÓN
La velocidad de reacción se define como la cantidad de sustancia que reacciona por unidad de tiempo. Por ejemplo, la oxidación del hierro bajo condiciones atmosféricas es una reacción lenta que puede tomar muchos años,[pero la combustión del butano en un fuego es una reacción que sucede en fracciones de segundo.
Se define la velocidad de una reacción química como la cantidad de sustancia formada (si tomamos como referencia un producto) o transformada (si tomamos como referencia un reactivo) por unidad de tiempo.
La velocidad de reacción no es constante. Al principio, cuando la concentración de reactivos es mayor, también es mayor la probabilidad de que se den choques entre las moléculas de reactivo, y la velocidad es mayor. a medida que la reacción avanza, al ir disminuyendo la concentración de los reactivos, disminuye la probabilidad de choques y con ella la velocidad de la reacción. La medida de la velocidad de reacción implica la medida de la concentración de uno de los reactivos o productos a lo largo del tiempo, esto es, para medir la velocidad de una reacción necesitamos medir, bien la cantidad de reactivo que desaparece por unidad de tiempo, bien la cantidad de producto que aparece por unidad de tiempo. La velocidad de reacción se mide en unidades de concentración/tiempo, esto es, en moles/s.
La teoría de colisiones
La teoría de colisiones, propuesta hacia 1920 por Gilbert N. Lewis (1875-1946) y otros químicos, afirma que para que ocurra un cambio químico es necesario que las moléculas de la sustancia o sustancias iniciales entren en contacto mediante una colisión o choque.
Pero no todos los choques son iguales. El choque que provoca la reacción se denomina choque eficaz y debe cumplir estos dos requisitos:
- Que el choque genere la suficiente energía para romper los enlaces entre los átomos.
- Que el choque se realice con la orientación adecuada para formar la nueva molécula.
Los choques que no cumplen estas condiciones y, por tanto, no dan lugar a la reacción, se denominan choques ineficaces.
A veces, el paso de reactivo a producto se realiza mediante la formación de un compuesto intermedio ocomplejo activado que se transformará posteriormente en los productos.
La energía de activación ( ) en química es la energía que necesita un sistema antes de poder iniciar un determinado proceso. La energía de activación suele utilizarse para denominar la energía mínima necesaria para que se produzca una reacción química dada. Para que ocurra una reacción entre dos moléculas, éstas deben colisionar en la orientación correcta y poseer una cantidad de energía mínima.
Factores que afectan a la velocidad de una reacción química
¿De qué depende que una reacción sea rápida o lenta? ¿Cómo se puede modificar la velocidad de una reacción? Una reacción química se produce mediante colisiones eficaces entre las partículas de los reactivos, por tanto, es fácil deducir que aquellas situaciones o factores que aumenten el número de estas colisiones implicarán una mayor velocidad de reacción. Veamos algunos de estos factores.
Temperatura
Al aumentar la temperatura, también lo hace la velocidad a la que se mueven las partículas y, por tanto, aumentará el número de colisiones y la violencia de estas. El resultado es una mayor velocidad en la reacción. Se dice, de manera aproximada, que por cada 10 °C de aumento en la temperatura, la velocidad se duplica.
Esto explica por qué para evitar la putrefacción de los alimentos los metemos en la nevera o en el congelador. Por el contrario, si queremos cocinarlos, los introducimos en el horno o en una cazuela puesta al fuego.
Grado de pulverización de los reactivos
Si los reactivos están en estado líquido o sólido, la pulverización, es decir, la reducción a partículas de menor tamaño, aumenta enormemente la velocidad de reacción, ya que facilita el contacto entre los reactivos y, por tanto, la colisión entre las partículas.
Por ejemplo, el carbón arde más rápido cuanto más pequeños son los pedazos; y si está finamente pulverizado, arde tan rápido que provoca una explosión.
Naturaleza química de los reactivos que intervienen en la reacción
Dependiendo del tipo de reactivo que intervenga, una determinada reacción tendrá una energía de activación:
- Muy alta, y entonces será muy lenta.
- Muy baja, y entonces será muy rápida.
Así, por ejemplo, si tomamos como referencia la oxidación de los metales, la oxidación del sodio es muy rápida, la de la plata es muy lenta y la velocidad de la oxidación del hierro es intermedia entre las dos anteriores.
Concentración de los reactivos
Si los reactivos están en disolución o son gases encerrados en un recipiente, cuanto mayor sea su concentración, más alta será la velocidad de la reacción en la que participen, ya que, al haber más partículas en el mismo espacio, aumentará el número de colisiones.
El ataque que los ácidos realizan sobre algunos metales con desprendimiento de hidrógeno es un buen ejemplo, ya que este ataque es mucho más violento cuanto mayor es la concentración del ácido.
La variación de la velocidad de reacción con los reactivos se expresa, de manera general, en la forma:
v = k [A]α [B]β
Donde α y β son coeficientes que no coinciden necesariamente con los coeficientes estequiométricos de la reacción general antes considerados. La constante de velocidad k, depende de la temperatura.
Catalizadores
Los catalizadores son sustancias que facilitan la reacción modificando el mecanismo por el que se desarrolla. En ningún caso el catalizador provoca la reacción química; no varía su calor de reacción.
Los catalizadores se añaden en pequeñas cantidades y son muy específicos; es decir, cada catalizador sirve para unas determinadas reacciones. El catalizador se puede recuperar al final de la reacción, puesto que no es reactivo ni participa en la reacción.
Para la reacción aA + bB que da rR+ sS, la velocidad de reacción es la rapidez con que se forman R y S (lo que es igual que la rapidez con la que desaparecen A y B).
Para la reacción
La velocidad de reacción es la rapidez con la que A y B se transforman en R y S
Para la reacción rR+ sS que da aA + bB, la velocidad de reacción es la rapidez con que se forman A y B (lo que es igual que la rapidez con la que desaparecen R y S).
Para la reacción
La velocidad de reacción es la rapidez con la que R y S se transforman en A y B
EQUILIBRIO QUÍMICO
¿Qué es el Equilibrio Químico?
Es un estado de cualquier sistema en el que exista al menos una reacción reversible y la concentración de cada especie no cambie conforme pase el tiempo.
Para que la concentración de cada especie que está presente en el sistema no cambie a pesar de la existencia de una o más reacciones, en cada reacción reversible la velocidad de la reacción que se desplaza hacia la izquierda debe ser igual a la velocidad de reacción que se desplaza hacia la derecha.
Estequiometría
2H2 + O2 à 2H2O
Una Reacción química es un proceso en el cual una
sustancia (o sustancias) desaparece para formar una o más sustancias nuevas.
Las ecuaciones químicas son el modo de representar a
las reacciones químicas.
Por ejemplo el hidrógeno gas (H2) puede reaccionar con
oxígeno gas(O2) para dar agua (H20). La ecuación química
para esta reacción se escribe:
El "+" se lee como "reacciona con"
La flecha significa "produce".
Las fórmulas químicas a la izquierda de la flecha representan las
sustancias de partida denominadas reactivos.
A la derecha de la flecha están las formulas químicas de las sustancias
producidas denominadas productos.
Los números al lado de las formulas son los coeficientes (el
coeficiente 1 se omite).
La estequiometría es
el cálculo entre relaciones cuantitativas entre los reactantes y productos
en el transcurso de una reacción química.
 La estequiometría es una herramienta indispensable en
la química. Problemas tan diversos como, por ejemplo, la medición de la
concentración de ozono en la atmósfera, la determinación del rendimiento
potencial de oro a partir de una mina y la evaluación de diferentes procesos
para convertir el carbón en combustibles gaseosos, comprenden aspectos de estequiometría.
La estequiometría es una herramienta indispensable en
la química. Problemas tan diversos como, por ejemplo, la medición de la
concentración de ozono en la atmósfera, la determinación del rendimiento
potencial de oro a partir de una mina y la evaluación de diferentes procesos
para convertir el carbón en combustibles gaseosos, comprenden aspectos de estequiometría.
El primero que enunció los principios
de la estequiometría fue Jeremias Benjamin Richter (1762-1807), en 1792.
Escribió:
La estequiometría es la ciencia que
mide las proporciones cuantitativas o relaciones de masa en la que los
elementos químicos que están implicados.
Principio científico
En una reacción química se
observa una modificación de las sustancias presentes: los reactivosse
modifican para dar lugar a los productos.
A escala microscópica, la reacción
química es una modificación de los enlaces entre átomos,
por desplazamientos de electrones: unos enlaces se rompen y otros se forman, pero
los átomos implicados se conservan. Esto es lo que llamamos la Ley
de conservación de la materia, que implica las dos leyes siguientes:
1.- la conservación del número de
átomos de cada elemento químico
2.- la conservación de la carga total
Las relaciones estequiométricas entre
las cantidades de reactivos consumidos y productos formados dependen
directamente de estas leyes de conservación, y están determinadas por la
ecuación (ajustada) de la reacción.
Ajustar o balancear una reacción
¿Qué significa ajustar o balancear una
reacción? Veamos.
Una ecuación química (que no es más que
la representación escrita de una reacción química) ajustada debe reflejar lo
que pasa realmente antes de comenzar y al finalizar la reacción y, por tanto,
debe respetar las leyes de conservación del número de átomos y de la carga
total.
Para respetar estas reglas, se pone
delante de cada especie química un número llamado coeficiente
estequiométrico, que indica la proporción de cada especie involucrada (se
puede considerar como el número de moléculas o de átomos, o de iones o de
moles; es decir, la cantidad de materia que se consume o se treansforma).
Por ejemplo:
En la reacción de combustión de metano (CH4),
éste se combina con oxígeno molecular(O2) del aire para
formar dióxido de carbono (CO2) y agua (H2O).
La reacción sin ajustar (sólo
representando los elementos que interactúan) será:
CH4 + O2 à CO2 + H2O
Esta reacción no es correcta, porque no cumple la ley de conservación de la materia. Para el elemento hidrógeno (H), por ejemplo, hay 4 átomos en los reactivos (CH4) y sólo 2 en los productos (H2O). Se ajusta la reacción introduciendo delante de las fórmulas químicas de cada compuesto un coeficiente estequiométrico adecuado.
De esta manera, si se pone un 2 delante
del H2O:
CH4 + O2 à CO2 + 2H2O
se respeta la conservación para el carbono (C) y el hidrógeno (H), pero no para el oxígeno (O), situación que puede corregirse poniendo otro 2 delante de O2 en los reactivos:
CH4 + 2O2 à CO2 + 2H2O
y se obtiene así, finalmente, la reacción ajustada.
Ésta dice que 1 molécula
de metano (CH4) reacciona con 2 moléculas de
oxígeno molecular (O2) para dar 1 molécula de
dióxido de carbono(CO2) y 2 moléculas de agua (H2O).
Si verificamos el número de átomos veremos que en ambos lados de la ecuación
hay 1 átomo de carbono (C), 4 átomos de hidrógeno (H) y 4 átomos de oxígeno
(O). La materia (la cantidad de átomos) se ha conservado una vez terminada la
reacción química.
martes, 21 de agosto de 2012
Actividad Experimental
Universidad Nacional Autonoma de Mexico
Plantel Vallejo
Objetivo:
Introducción: La industria Química es el sector que se ocupa de las transformaciones químicas a gran escala. La industria química se ocupa de la extracción y procesamiento de las materias primas, tanto naturales como si.La Metalúrgica es la obtención de metales (acero, cobre, aluminio) a partir de sus menas naturales. La Petroquímica se ocupa de los productos derivados del petróleo y su utilización.
Procedimiento: Desarmamos el objeto por completo (en este caso una chapa), posteriormente clasificamos que tipo de metal era cada una de las partes dividiéndolas por grupos, en seguida tomamos el peso de cada uno de ellos. Y por último, procedimos a tomar su volumen correspondiente, esto fue, llenando probetas con determinada cantidad de agua para después introducir dentro de la probeta un grupo de metal; con esto, con el aumento de agua en la probeta determinamos el volumen total de cada uno de los grupos.
Resultados:
Analisis de Resultado: La tabla que presentamos indica el peso y el volumen de los 4 grupos que formamos con los metales de la chapa que fue el acero inoxidable, hierro, cobre y la estructura.
Conclusiones: A la hora de pesar los metales nos dimos cuenta de que su peso de cada grupo era diferente al igual que el volunen de estos grupos que formamos, con este ejercicio observamos que tan solo una chapa de nuestra casa tiene diferentes tipos de metales ahora imaginemos cuantas cosas no tenemos en diferentes lugares de nuestro hogar que son metales, es interesante conocer como son y como es su fabricacion ya que en nuestra casa tenemos muchos de estos minerales o aleaciones y no sabemos como es su origen, lo interesante que son y lo dificil que a veces es fabricarlos.
Saber aplicar nuestros conocimientos, viendo la composición de la estructura de un objeto cualquiera; clasificando tipos de metales y sabiendo su peso y volumen exactos que lo componen.
Introducción: La industria Química es el sector que se ocupa de las transformaciones químicas a gran escala. La industria química se ocupa de la extracción y procesamiento de las materias primas, tanto naturales como si.La Metalúrgica es la obtención de metales (acero, cobre, aluminio) a partir de sus menas naturales. La Petroquímica se ocupa de los productos derivados del petróleo y su utilización.
Procedimiento: Desarmamos el objeto por completo (en este caso una chapa), posteriormente clasificamos que tipo de metal era cada una de las partes dividiéndolas por grupos, en seguida tomamos el peso de cada uno de ellos. Y por último, procedimos a tomar su volumen correspondiente, esto fue, llenando probetas con determinada cantidad de agua para después introducir dentro de la probeta un grupo de metal; con esto, con el aumento de agua en la probeta determinamos el volumen total de cada uno de los grupos.
Resultados:
VOLUMEN
|
PESO
|
|
Grupo 1
acero inoxidable |
51ml
|
88.9g
|
Grupo 2
hierro |
2ml
|
17g
|
Grupo 3
cobre |
20ml
|
138.2g
|
Grupo 4
estructura |
20ml
|
148g
|
Analisis de Resultado: La tabla que presentamos indica el peso y el volumen de los 4 grupos que formamos con los metales de la chapa que fue el acero inoxidable, hierro, cobre y la estructura.
Conclusiones: A la hora de pesar los metales nos dimos cuenta de que su peso de cada grupo era diferente al igual que el volunen de estos grupos que formamos, con este ejercicio observamos que tan solo una chapa de nuestra casa tiene diferentes tipos de metales ahora imaginemos cuantas cosas no tenemos en diferentes lugares de nuestro hogar que son metales, es interesante conocer como son y como es su fabricacion ya que en nuestra casa tenemos muchos de estos minerales o aleaciones y no sabemos como es su origen, lo interesante que son y lo dificil que a veces es fabricarlos.
sábado, 18 de agosto de 2012
¿Cómo contribuye a el Producto Interno Bruto?
¿COMO CONTRIBUYE AL PRODUCTO INTERNO
BRUTO?
 El PIB representa la suma de todos
los bienes y servicios finales producidos en un país durante un año,
ya sea por nacionales o por extranjeros residentes.
El PIB representa la suma de todos
los bienes y servicios finales producidos en un país durante un año,
ya sea por nacionales o por extranjeros residentes.
Bienes
y servicios: vehículos, ropas, alimentos, vivienda, electrodomésticos, consulta
del dentista, minuta del abogado, servicio de seguridad, servicio de limpieza,
entradas del cine, corte de pelo, etc.
Finales: no se incluyen los bienes
intermedios ya que posteriormente se incorporarán a un bien final. Si se
contabilizaran los bienes intermedios se produciría una doble contabilización.
Los componentes del PIB son:
Gasto de Consumo Personal, esto
significa que una familia o persona compra o utiliza algún bien o servicio
final producido en el país durante el último año. Y se dividen en:
Bienes Duraderos, que son los que duran más de un año y
en:
Bienes Perecederos, y son los que
duran menos de un año.
Inversión Privada Bruta, esto es cuando por ejemplo una
familia compra una casa nueva.
Gasto del Gobierno, es cuando el gobierno construye
infraestructura necesaria para el desarrollo del país.
Exportaciones, todos los bienes y servicios finales que produce el país y
sevende al extranjero.
Inversión Privada, cuando las empresas extranjeras invierten ya sea estableciéndose
en el país ó aportando dinero a empresas ya establecidas en México.
El PIB. se obtiene con aplicando
la siguiente fórmula:
PIB. = C + I + G + X – M
PIB = consumo + inversión + gasto público + exportaciones - importaciones
PIB = consumo + inversión + gasto público + exportaciones - importaciones
¿Qué es Química Industrial?
 Química Industrial es la rama de la química que aplica los conocimientos químicos a la
producción de forma económica de materiales y productos
químicos especiales con el mínimo impacto adverso sobre el medio
ambiente.
Química Industrial es la rama de la química que aplica los conocimientos químicos a la
producción de forma económica de materiales y productos
químicos especiales con el mínimo impacto adverso sobre el medio
ambiente.
INDUSTRIA QUÍMICA
Sector que se ocupa de las transformaciones
químicas a gran escala. La industria química se ocupa de la extracción y
procesamiento de las materias primas, tanto naturales como sinteticas.
Existen dos tipos de industria química:
Industria química de base: Utilizan estas materias primas básicas y elaboran
productos intermedios que, a su vez, sirven de materia prima para otras
industrias
Industrias químicas de transformacion: Están destinadas al consumo directo de las
personas, emplean como materias primas los productos elaborados por
las industrias químicas de base.
Tipos de industrias químicas
·
Metalúrgica. Obtención de metales (acero, cobre, aluminio) a partir de sus menas naturales.Petroquímica. Se ocupa de los productos derivados del petróleo y su utilización.
Metalúrgica. Obtención de metales (acero, cobre, aluminio) a partir de sus menas naturales.Petroquímica. Se ocupa de los productos derivados del petróleo y su utilización.
·
Agrícola. Fabricación de abonos,
insecticidas, pesticidas y otros productos similares.
·
Farmacéutica. Investigación, preparación
y comercialización de toda clase de medicamentos.
·
Alimentaria. Preparación de alimentos y
su conservación.
·
Textil. Obtención de fibras que se
transforman en tejidos.
·
Materiales
de construcción. Fabricación de
cementos, cerámicas, yesos, pinturas, etc.
·
Productos
intermedios. Obtención de
ácido sulfúrico, amoniaco, etc., utilizados por otras industrias.
Suscribirse a:
Entradas (Atom)







