UNIVERSIDAD NACIONAL AUTÓNOMA DE MÉXICO
COLEGIO DE CIENCIA Y HUMANIDADES PLANTEL VALLEJO
ACTIVIDAD EXPERIMENTAL
Objetivo:Comprobar y conocer el pH de los materiales a explorar.
Introducción: El pH (potencial de hidrógeno) es una medida de acidez o alcalinidad de una disolución. El pH indica la concentración de iones hidronio [H3O+] presentes en determinadas sustancias.
Escala de pH
Los ácidos y las bases tienen una característica que permite medirlos: es la concentración de los iones de hidrógeno (H+). Los ácidos fuertes tienen altas concentraciones de iones de hidrógeno y los ácidos débiles tienen concentraciones bajas. El pH, entonces, es un valor numérico que expresa la concentración de iones de hidrógeno.
Hay centenares de ácidos. Ácidos fuertes, como el ácido sulfúrico, que puede disolver los clavos de acero, y ácidos débiles, como el ácido bórico, que es bastante seguro de utilizar como lavado de ojos. Hay también muchas soluciones alcalinas, llamadas "bases", que pueden ser soluciones alcalinas suaves, como la Leche de Magnesia, que calman los trastornos del estómago, y las soluciones alcalinas fuertes, como la soda cáustica o hidróxido de sodio, que puede disolver el cabello humano.
Los valores numéricos verdaderos para estas concentraciones de iones de hidrógeno marcan fracciones muy pequeñas, por ejemplo 1/10.000.000 (proporción de uno en diez millones). Debido a que números como este son incómodos para trabajar, se ideó o estableció una escala única. Los valores leídos en esta escala se llaman las medidas del "pH".
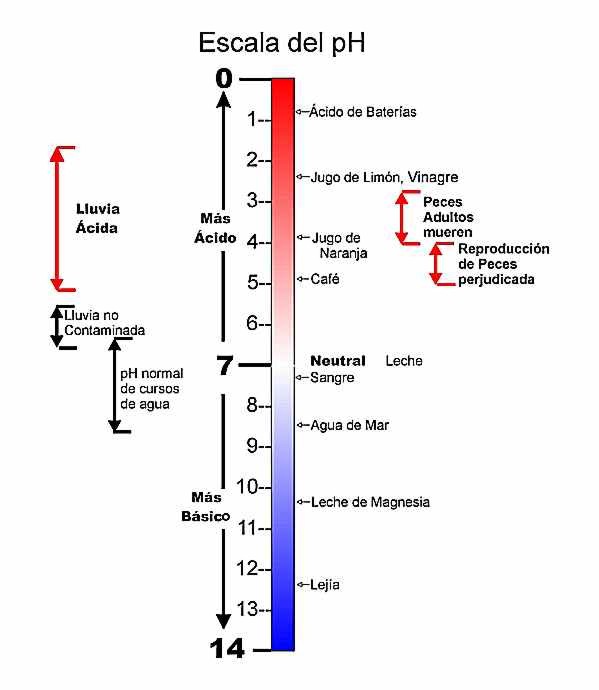 |
• La escala pH está dividida en 14 unidades, del 0 (la acidez máxima) a 14 ( nivel básico máximo). El número 7 representa el nivel medio de la escala, y corresponde al punto neutro. Los valores menores que 7 indican que la muestra es ácida. Los valores mayores que 7 indican que la muestra es básica.
• La escala pH tiene una secuencia logarítmica, lo que significa que la diferencia entre una unidad de pH y la siguiente corresponde a un cambio de potencia 10. En otras palabras, una muestra con un valor pH de 5 es diez veces más ácida que una muestra de pH 6. Asimismo, una muestra de pH 4 es cien veces más ácida que la de pH 6.
Materiales:
- 10 sustancias de uso común
- Tubos de ensalle y base
- Laminas pH
- Agua destilada
Procedimiento: En cada tubo de ensalle se vierte la sustancia y se le agrega agua destilada. Debe hacerse una mezcla homogénea, si es necesario se tiene que agitar hasta conseguir la mezcla.
Una vez finalizada esta etapa, procedemos a tomar una de las laminillas pH, vertir en el tubo en que se encuentra la sustancia, esperar el resultado.
La laminilla marcara una serie de colores y con ellos sabremos cual es el pH de cada sustancia.
Evidencia Fotográfica:
Análisis de Resultados:
Sustancias a las cuales calculamos su pH:
- Perfume ------- 5
- Alcohol----------6
- Vinagre----------2
- Aceite------------6
- Suavitel---------10
- Shampoo-------6
- Crema Corporal 6
- Enjuague Capilar 5
- Agua-------------7
- Jabón de Manos 6
- Yogurt bebible 4
Conclusión: Debemos saber el pH de las cosas básicas de nuestro uso cotidiano para tener o estar equilibrados.


No hay comentarios:
Publicar un comentario